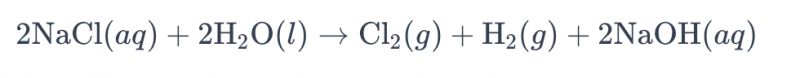Prosés éléktrolisis larutan brine nganggo éléktroda titanium pikeun ngahasilkeun klorin umumna disebut "éléktrolisis brine." Dina prosés ieu, éléktroda titanium dianggo pikeun ngagampangkeun réaksi oksidasi ion klorida dina brine, anu ngarah kana generasi gas klorin. Persamaan kimia sakabéhna pikeun réaksi ieu nyaéta sapertos kieu:
Dina persamaan ieu, ion klorida ngalaman oksidasi di anoda, ngahasilkeun gas klorin, sedengkeun molekul cai diréduksi di katoda, ngahasilkeun gas hidrogén. Salian ti éta, ion hidroksida ngalaman réduksi di anoda, ngabentuk gas hidrogén sareng natrium hidroksida.
Pilihan éléktroda titanium disababkeun ku résistansi korosi sareng konduktivitas titanium anu saé pisan, anu ngamungkinkeun éta ngalaman réaksi sacara stabil nalika éléktrolisis tanpa korosi. Ieu ngajantenkeun éléktroda titanium pilihan anu idéal pikeun éléktrolisis cai uyah.
Éléktrolisis cai asin biasana meryogikeun sumber daya éksternal pikeun nyayogikeun énergi pikeun réaksi éléktrolitik. Sumber daya ieu biasana mangrupikeun catu daya arus searah (DC) sabab réaksi éléktrolitik meryogikeun arah aliran arus anu konsisten, sareng catu daya DC tiasa nganteurkeun arah arus anu konstan.
Dina prosés éléktrolisis cai asin pikeun ngahasilkeun gas klorin, catu daya DC tegangan rendah umumna dianggo. Tegangan catu daya gumantung kana kaayaan réaksi khusus sareng desain alat, tapi umumna antara 2 dugi ka 4 volt. Salian ti éta, inténsitas arus catu daya mangrupikeun parameter penting anu kedah ditangtukeun dumasar kana ukuran ruang réaksi sareng hasil produksi anu dipikahoyong.
Singkatna, pilihan catu daya pikeun éléktrolisis cai asin gumantung kana sarat khusus tina ékspérimén atanapi prosés industri pikeun mastikeun réaksi anu efisien sareng kahontalna produk anu dipikahoyong.
Waktos posting: 16-Jan-2024